„Eine solche direkte Kopplung hat es bisher noch nicht gegeben“, sagt Projekt-Koordinator Dr. Henrik Junge, Themenleiter am Likat. Das Konzept kann die Energiewende auf dem Lande wesentlich beschleunigen: Es erlaubt Unternehmen und Kommunen sich vom Windkraftaufkommen unabhängig mit „grünem“ Strom zu versorgen.
Speicher für Wasserstoff
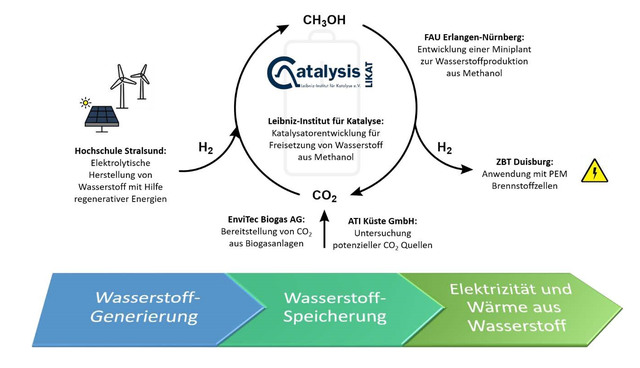
Mit diesem Strom aus erneuerbaren Energien wird aus Wasser elektrolytisch Wasserstoff erzeugt, der wiederum mit CO2 in Methanol umwandelt wird. Methanol, einfachster Vertreter in der Gruppe der Alkohole, fungiert somit als Speicher für Wasserstoff, wie es Chemiker seit langem vorschlagen. Dr. Junge: „Methanol lässt sich im Unterschied zu Wasserstoff gut handhaben und auch über weite Strecken transportieren.“ Bei Bedarf wird Methanol in H2 rückverwandelt und direkt im Anschluss in einer Brennstoffzelle zur Stromerzeugung genutzt.
Testanlage mit 500 Stunden Laufzeit
Im Forschungsverbund Metha-Cycle unter Leitung des Likat nutzten die Partner ausserdem die Abwärme der Brennstoffzelle, um der Wasserstoff-Rückgewinnung einen Teil der nötigen Reaktionswärme zuzuführen. Die Testanlage der Friedrich-Alexander-Universität (FAU) Erlangen-Nürnberg hat im Frühjahr mit knapp 500 Stunden Laufzeit die Funktionstüchtigkeit des Konzepts demonstriert. Die Brennstoffzelle, entwickelt vom Zentrum für Brennstoffzellentechnik (ZBT) Duisburg, produzierte kontinuierlich Strom mit einer Leistung bis zu 39 Watt.
Fördersumme: 1.8 Mio Euro
Üblicherweise braucht es hohen Druck und Temperaturen von mehreren hundert Grad Celsius, um aus dem Methanol wieder den Wasserstoff zu gewinnen. Das machte eine allgemeine Anwendung im Rahmen von Energiekonzepten bisher wenig attraktiv. 2013 beschrieben Likat-Chemikerinnen und Chemiker dann im Magazin Nature, wie sie mithilfe eines Ruthenium-Katalysators bei milden Bedingungen unter hundert Grad Celsius aus einer wässrigen Methanollösung H2 und CO2 erzeugten. Diese Reaktion galt es nun zu optimieren. Denn um eine Brennstoffzelle dauerhaft befeuern zu können, muss der chemische Prozess ausreichend H2 pro Zeiteinheit zur Verfügung stellen, und dies auch in gewisser Reinheit.
Zu diesem Zweck nahm sich die Forschungsgruppe um Dr. Junge und Likat-Direktor Prof. Dr. Matthias Beller vor, die molekularen Abläufe der Reaktion zu analysieren. Mit Partnern für ein Verbundprojekt war Henrik Junge schon im Gespräch, und zwar mit dem Ziel, „das Aufkommen regenerativer Energie von ihrem Verbrauch zu entkoppeln“, wie er sagt. Inzwischen begann alle Welt über die Rolle von Wasserstoff und Methanol für eine Energiewende zur Rettung des Klimas nachzudenken. Im Herbst 2016 übernahm das BMWi die Förderung des Projektes Metha-Cycle für dreieinhalb Jahre mit einem Gesamtumfang von insgesamt 1,8 Millionen Euro.
„Mechanistische“ Analysen
Für ihren Teil analysierten die Likat-Forschenden, wie der Ruthenium-Katalysator in der Methanollösung arbeitet, um zu H2 und CO2 zu kommen, also den Wasserstoff wieder freizusetzen. Bei diesen „mechanistischen Untersuchungen“, wie sie die Arbeiten nennen, entdeckten sie drei kaskadenartig verbundene Schritte. Am Ende der ersten beiden Schritte entsteht jeweils schon ein Teil des Wasserstoffs und zusätzlich ein Zwischenprodukt, ein sogenanntes Intermediat. Im ersten Schritt ist es Formaldehyd, das im Beisein des Katalysators dann im zweiten Schritt weiterverarbeitet wird. Im zweiten Schritt der Kaskade entsteht dann Ameisensäure, und mit der kennt sich das Likat bestens aus. Denn vor 20 Jahren war es den Rostockern gelungen, aus Ameisensäure bei Raumtemperatur H2 zu gewinnen.
Doch ausgerechnet der dritte Schritt, der von der Ameisensäure zu Wasserstoff, erwies sich als der langsamste, wie Henrik Junge sagt. „Er bremste das gesamte System.“ So hätte die Brennstoffzelle nicht schnell genug Nachschub an H2 bekommen. Um die Kaskade auf Trab zu bringen, entschieden die Forscher sich letztlich für ein bi-katalytisches System: sie gaben ihrem Ruthenium-Katalysator als Helfer einen zweiten Katalysator an die Seite. Überraschenderweise brauchten sie dazu ihren ersten Katalysator nur etwas zu modifizieren.
Letzter Schliff in Erlangen
Ebenso überrascht wurden die Chemikerinnen und Chemiker vom synergetischen Effekt ihres Systems. Dr. Junge: „Im Zusammenschluss ermöglichten die beiden Katalysatoren eine bessere Ausbeute, als die Summe ihrer Einzelleistung erbracht hätte.“ In Erlangen machten die beteiligten Verfahrenstechnikerinnen und –techniker an der FAU den Bi-Katalysator für einen kontinuierlichen Prozess in der Testanlage fit, mit der das Forschungskonsortium von Metha-Cycle die Funktionstüchtigkeit des Konzepts letztlich unter Beweis stellte. Dazu imprägnierten sie einen festen hochporösen Träger mit dem katalytisch aktiven Komplex aus Rostock. Über diesem Träger fliessen kontinuierlich Methanol- und Wasserdampf. Ebenso kontinuierlich wird der entstandene Wasserstoff abgeleitet, um in der angeschlossenen Brennstoffzelle sofort verstromt zu werden.
Literatur: C. H. Schwarz, A. Agapova , H. Junge, M. Haumann, Catalysis Today 2020,342, 178-186; Immobilization of a selective Ru-pincer complex for low temperature methanol reforming – material and process improvements.
Text: Leibniz-Institut für Katalyse (Likat)






1 Kommentare
Huh? Andere Forschungsinstitute und Unternehmen bemühen sich um das genaue Gegenteil, nämlich um den "Power-to-Liquid"-Prozess, bei dem elektrolytisch "grün" produzierter Wasserstoff in den flüssigen Brennstoff Methanol umgewandelt und der Umgebungsluft dabei CO2 entzogen wird!
Beim Umkehrprozess muss zwangsläufig CO2 freigesetzt werden ... wohin damit? Wie steht es mit der Gesamt-Ökobilanz? Mit dem Gesamt-Wirkungsgrad? Noch fühle ich mich außerstande, dem Projekt den Stempel "sinnvoller Baustein der Energiewende" aufzudrücken!